|
Руды Mg – представляют различные природные соединения минералов Mg и пустых пород.
К ним относится:
Белый минерал 1. Магнезит – MgCO3 углекислая соль Mg
Черная порода 2.Доломит - MgCO3 СаСО3 двойная углекислая соль Mg и Са.
Гидравлическое вещество
розового, серого, желтого цвета. 3. Карналлит – MgCl2 + KCl + 6H2O
шестиводный двойной хлорид Mg и калия
Переработка руд: 1. Обжиг t = 800-900 0
MgCO3 → MgО + СО2 для разложения
800
минералов
2. Механическое обогащение дробление и сортировка
3. Гидрохимическая обработка – выщелачивание металлов из руд
Mg получают:
электролитическим термическим способом
электролиз Mg включает:
1. Получение хлоридов Mg – чистых безводных
2. электролиз солей
3. рафинирование
I этап.
1. Получение MgCl проводят:
обезвоживанием хлорированием
Обезвоживание хлорных солей Mg проводят в трубчатых вращающихся печах l = 40 м. о 3 м. t = 220 – 420 0 – где испаряется Н2О.
MgCl2 + KCl + 6H2O → MgCl2. 6H2O→ MgCl2 → разбавлен в 3-х фазных электрических печах t = 750 – 800 0
2 стадия – если руда магнезит или доломит, то она измельчается и перемешивается с графитом, прессуется в брикеты, которые загружаются в электрическую печь с t = 800- 900 0 с хлором, что приводит к образованию MgCl2.
II этап. Электролиз Mg (c 3% примесей) проводят в ваннах 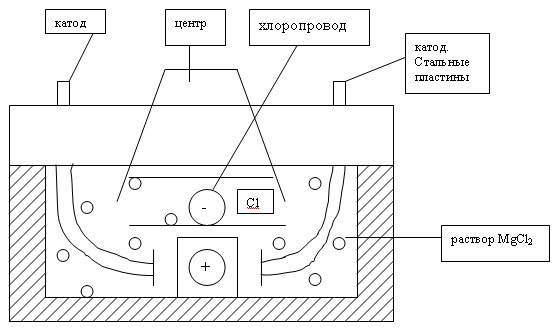 Ванна стальная, выложенная, шамотный киричом, с плотной крышкой.
Электролит – расплавленный MgCl2 – анод (+), графитовый, катод (-), KCl; CaCO2 – придают вес электролиту и обеспечивают высокую электропроводимость.
х = 5 – 5,6 В I = 50000А. Ванна работает непрерывно 12-14 месяцев, затем на ремонт.
Расход: 1 т. Mg = 4,5 т. MgCl2
25 кт. анодов
18000 кВт./ч. электрической энергии
Mg извлекается вакуумным ковшом 2-3 раза в сутки; на дне шлам
III этап – рафинирование – очистка примесей и получение Mg 99,99%
Переплав со взгонкой специальными флюсами -> сплав фтористых и хлористых солей.
Флюс подбирает так, что они соединяясь с примесями образуют шлак с t пл. = 710 – 690 0 (t Mg = 651), поэтому по мере остывания расплава образуется корка шлака. Шлак пробивают и Mg разливают в слитки.
2 способ рафинирование возгонкой:
Mg – сырец (с примесями) подвергают сублимации (возгонки) в глубоком вакууме (0,1 – 0,2 мм. рт. ст.) при t =600 0
Спираль сопротивления - нагрева
|
|
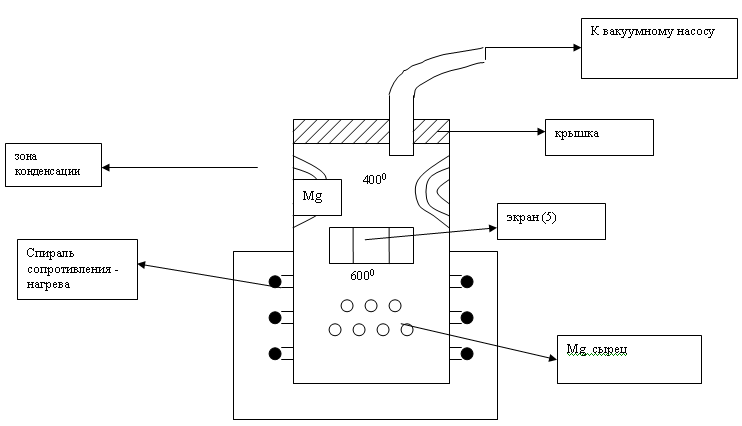
Mg – сырец загружают в стальную реторту, герметически закрытой крышкой. Через верхнюю трубку из реторты откачивается воздух. Нижняя часть реторты в нагревателе где Mg – сыр. t =600 0, при нагреве Mg испаряется и пары его поднимаются вверх и попадают в зону конденсации (охлаждения) (осаждения) Mg оседает на стенках, а затем его собирают и переплавляют в слитки.
Термический способ получения Mg проводят с помощью восстановителей Si (селикотермически) и С (карботермически).
Этапы: 1. подготовка исходных материалов
2. Восстановление Mg, возгонка и конденсация
3. Расплавление чистого Mg и разливка в слитки
Доломит = FeSi ферросилицием и брикеты → смесь помещают в реторту
=> выкачивают воздух (Р=0,1 мм. рт. ст.). Смесь нагревают до t = 1150 – 1170 0, под действием которых Mg восстанавливается:
2 MgO + 2CaO + FeSi = 2CaO*SiO2 + 2 Mg + Fe
Пары Mg в конденсаторе осаждаются на стенках стального цилиндра Mg переплавляют в слитки.
Карботермический способ
Доломит соединяется с карбонатом
Са как и в I способе – Si.
MgO + CaC2 = Mg + CaO + 2C
Реторта работает 10 часов; емкость = 100 кг. Производительность = 600 – 700 кг. в сутки
|